马益民医生的科普号
- 精选 手术后癌细胞并没有扩散,为什么还要化疗?医生说出心里话
https://ma.mbd.baidu.com/r/wi5kzr7?f=cp&u=30ef08a0 39健康网 04-17 15:1439健康网官方帐号 相信不少癌症患者会有这样的困惑:明明做完肿瘤切除手术,身体恢复得不错,复查后的病理也显示癌细胞并没有扩散,却被医生告知需要进行放化疗,到底是为什么?有没有必要? 今天就和大家一起来聊一聊这个话题。 肿瘤切除,不等于治疗结束 在很多人的理解中,手术是将肿瘤病灶彻底切除,能让患者获得根治的有效途径。这个说法不能说错,但也不全对。 通过手术,的确可以切除肉眼可见的成形肿瘤病灶。但恶性肿瘤多为浸润性生长,存续期间会侵袭、破坏周围组织,切除病灶后,体内可能会残留少部分微小肿瘤组织、细胞。 ? 其次,很多恶性肿瘤会通过血管和淋巴扩散转移至别处,以现在的医学手段很难彻底检查出所有隐藏起来的微小病灶,手术的刺激和术后免疫力降低,都可能刺激肿瘤细胞增殖,埋下日后复发的隐患。 更麻烦的是,因为手术的影响,体内的激素与环境出现变化,可能也会激活休眠的静止病灶。已有研究发现,进行肝脏切除手术后,余下组织再生过程中出现了某些癌基因过量表达的情况[1]。 如此看来,做完手术并不等于万事大吉。术后采取放化疗,核心是要杀死癌症病人体内潜藏的癌细胞,是降低肿瘤复发风险的重要手段。 放化疗会产生一定的毒副作用 ? 术后要不要进行放化疗治疗、如何进行,医生往往要结合肿瘤部位、分期、临床病理报告、病人身体状况等等做出决定,患者可以与医生进行沟通,听从医生的指导和建议。 不过,放化疗的确也是一种“杀敌一千自损八百”的行为,在杀灭癌细胞的同时,也会造成正常细胞损伤,或多或少会产生一定的毒副作用和不良反应,如食欲下降、恶心呕吐、腹痛腹泻、嗜睡、精神萎靡、周身乏力、免疫功能缺陷或下降、脱发等常见问题。 此外,随着化疗次数增加,毒副作用也会增强,诸多不良反应往往会让癌症患者承受身体和精神的双重痛苦,也让即将接受放化疗的癌症患者心生恐惧。 这样做,放化疗期间能好受点 为对抗可能产生的副作用,减少不良反应,减轻痛苦,加快恢复,以下做法值得尝试: ? 增加营养 放化疗期间部分癌症患者会以肉眼可见的速度消瘦,食欲不太好,只有保证充足的营养,身体才能有较强的抵抗力并能接受各种治疗。 因此,格外需要增加营养弥补消耗,维持正常的身体运转。饮食上,坚持“三高一多”的饮食原则,尽量吃一些高能量、高蛋白、高维生素的食物,如牛奶、鸡蛋、瘦肉、鱼肉、米面、大豆及制品、蔬菜水果,同时多饮水,促进排毒。 改善进食环境,饭前洗脸漱口,让病人和家人一起吃饭等,也是增进食欲的办法之一。当出现恶心、呕吐等症状时,则宜采用“间隙疗法”,进食清淡、易消化的食物,避开肥厚油腻,注意少食多餐。 如果身体条件允许,还可进行一些力所能及的简单锻炼,也可以一定程度上转移注意力、增加食欲。 中药缓解 针对放化疗引起的免疫力低下、食欲不振、恶心呕吐等问题,中医多采取扶正祛邪的方法。 此外,现代药理学研究也证明,中药可以通过促进肿瘤细胞凋亡、调节机体免疫功能和直接杀死肿瘤细胞等途径来达到抗肿瘤的疗效[2]。与西医的手术、放疗、化疗进行有机结合,可以明显改善癌症患者的生存质量。 针对抗放化疗期间出现的疲劳、乏力、精神不振问题,常采用补气中药,党参、黄芪,具有补气固表之效。 针对化疗药物导致头发稀疏、脱发的年轻人或女性,可服用黄精,补益精血、养血生发。 放疗导致的口干、烦躁,可使用玉竹、南北沙参、石斛等养阴生津的药物皆有利于缓解症状。 ? 针对放化疗引起的恶心、呕吐、食欲不振等副作用,素有仙草之称的灵芝,可以固本扶正、滋安补神,减轻副作用影响。此外,31年只钻研灵芝种植与研究的仙芝楼,曾联合国家食用菌加工技术研究分中心共同研究,灵芝孢子破壁前后在人体消化系统内的差异实验。结论指出,灵芝孢子破壁后其有效成分更易于在人体消化环境内释放[3]。 面对既定事实,焦虑和害怕都于事无补。听从医生指导,吃好喝好睡好,以积极健康的心态和主动的态度去面对,才是关键。
马益民 主任医师 江苏省人民医院 骨肿瘤科3896人已读 - 精选 骨肉瘤
第19章 骨肉瘤概述骨肉瘤曾经是一种致命的骨的恶性肿瘤,造成超过80%的患者在诊断后5年内死亡。随着对于这种疾病认识水平的提高,现在的治疗方案可以治愈大约70%的原发肢体肿瘤而无转移表现的患者。经典的骨肉瘤被定义为高度恶性的梭形细胞肉瘤并可产生骨样基质。全美每年大约可以诊断900例骨肉瘤,是除多发性骨髓瘤以外最常见的骨的原发恶性肿瘤。骨肉瘤的发生率在美国约为3/10,000。在骨肉瘤数据库中有超过10,000例的登记病例,在麻省总医院(Massachusetts General Hospital, MGH)的肿瘤中心自1972年来共诊断了670例此类病例。骨肉瘤更常见于男性患者,主要好发于生命过程的第二个十年里,其第二个好发高峰在成人的晚期,主要是由于与Paget’s病相关的骨肉瘤。骨肉瘤的病因目前还不清楚(与绝大多数其它骨肿瘤一样)。当有家族成员得了骨肉瘤,应考虑是否有遗传学的因素。对于遗传性的视网膜母细胞瘤和Li-Fraumeni综合症的患者更易并发骨肉瘤。病毒诱发骨肉瘤的证据在于动物实验证明,特定的病毒可以在所选择的动物身上诱发各种骨的肉瘤。放射引起的骨肉瘤占总数的3%,多见于其它类型肿瘤患者应用放射治疗和烷化剂治疗的情况。继发性的骨肿瘤的风险性见于,增加药物的剂量,化疗方案中烷化剂的应用可以潜在的增强放射效应从而继发骨肉瘤。对于受侵犯的骨应用放疗治疗比其它组织更易于继发肉瘤的产生。快速生长的肿瘤的好发部位与发病患者的年龄提示这种肿瘤的病理与骨的生长发育紧密相关。骨肉瘤好发于长骨的干骺段。其中最常见的部位是远端股骨,近端胫骨和肱骨,这些都是青少年生长发育最快的部位。扁骨较少累及。在MGH患者组的研究中,最常见的部位是膝关节(其中远端股骨,32%;近端胫骨,16%)。高度恶性的骨肉瘤应该被认作一种系统性的疾病,因为在做出诊断时多数已有微小转移灶的存在。无转移的患者在化疗和手术切除后一年或更长时间出现了新发肺部转移,其预后要好于那些在诊断时就有肺部转移灶的病人。大约有10%-20%的骨肉瘤患者在诊断时就有了转移的影像学表现,这类患者根据肌肉骨骼系统肿瘤协会的分期标准(Musculoskeletal Tumor Society, MSTS)归为III期骨肉瘤。在MGH的骨肉瘤患者中,大多数的患者(73%)为MSTS IIB期的肿瘤,12%的患者存在远处转移。这些转移灶的部位常通过胸部CT扫描和全身骨扫描来进行检测。转移灶的部位包括肺,其次是骨,更为少见的部位包括其它一些内脏器官,如胸膜、心包、肾、肾上腺、淋巴结和脑。少数患者存在骨和肺部的转移,转移造成的死亡多数肺部病灶控制的失败,如肺内的广泛转移,肺内出血,气胸,或腔静脉的阻塞等。绝大多数死于肿瘤转移的患者在死亡时都有肺的受累。临床表现患者通常存在疼痛和局部的软组织肿块。症状可以存在3个月或更长的时间,并且开始于一次受伤后。创伤并不认为是肿瘤的诱发因素,虽然许多的研究者试图证明创伤后的微小骨折可以诱导肿瘤的形成。症状可以时轻时重,导致诊断的困难。伴随的疼痛持续而逐渐加重。疼痛可以在休息时或夜间存在,并且与活动无关。常常没有全身性的症状。最重要的体检发现是软组织肿块的存在。软组织肿块的大小差别很大,但通常相当大并且可以触及。可以存在关节内的渗出,或存在有病理性骨折。特定的实验室检查常常是异常的,如碱性磷酸酶或乳酸脱氢酶水平,两者在诊断时可以是升高的。异常的升高,尤其是乳酸脱氢酶,常常提示预后不良。影像学表现在大多数的病例,影像学表现和临床信息可以帮助预测肿瘤的病理学诊断。骨肉瘤的典型的影像学表现显示为位于长骨干骺端的侵袭性病损。肿瘤破坏正常的骨小梁结构,边界不清,没有任何可见的骨内膜的骨反应。显见的放射线高密度的成骨区和低密度的溶骨区相混合。骨膜新生骨形成并升起于皮质表面,伴有Codman三角形成和“星放射状”表现。相关的软组织肿块有不同程度的骨化,取决于成骨和成软骨区域的范围。(Fig.1)病理学表现骨肉瘤被经典的定义为由高度恶性的肉瘤样基质和恶性成骨细胞直接产生肿瘤性骨样组织或骨的一类肿瘤。肿瘤常出现中心矿化,周围为不成熟的,缺乏矿化的骨组织,肿瘤细胞常出现间变,伴有异型细胞核和双着丝点。肿瘤可以有向成软骨细胞或成纤维细胞分化的区域,但只要存在小片区域的肿瘤骨样基质区域就可以诊断为骨肉瘤。(Figs.2,3)肿瘤分期骨肉瘤的分期与其它的高度恶性肉瘤相同。需要进行彻底的组织学和体格检查。血液学检查,包括要了解乳酸脱氢酶和碱性磷酸酶水平。此外需行包括病变部位骨和胸部平片检查,全身骨扫描,胸部CT扫描,局部MRI检查。MRI可能是决定是否可以施行保肢术或必须行截肢术以达到局部控制的最为重要的检查。冠状位T1相可以显示肿瘤髓腔内侵犯的范围。整个骨都需要被扫描到以排除骨内的跳跃转移灶。关节需要仔细评估有无肿瘤的侵犯。给予强化造影剂(钆)后的动态显像有助于了解术前化疗后肿瘤坏死的范围。肿瘤的分类本章节重点讨论经典的,高度恶性的,中心型骨肉瘤,但还有一些其它的类型。骨肉瘤根据其恶性程度分级,肿瘤部位数量,位于骨的部位不同和发病原因可以分为多种不同的亚型。表面型骨肉瘤的组织学分级就可以分为高度、中间型、或低度恶性。骨旁骨肉瘤典型的骨旁骨肉瘤表现为由组织学低度恶性的成纤维细胞组成的,产生编织样或层状的成骨。发病年龄比典型的骨肉瘤要大,多见于20-40岁之间。远端股骨后方是最常见的骨旁骨肉瘤的好发部位,其它长骨也可以受侵犯。肿瘤为来源于皮质骨的基底广泛的病变。病变后期肿瘤可以侵入皮质骨进入髓腔。治疗以外科手术切除为主,生存率为80%-90%。(Fig.4)骨膜骨肉瘤所谓骨膜骨肉瘤是一种中度恶性程度的成软骨细胞来源的表面骨病损,好发于胫骨近端。发病年龄与经典型骨肉瘤相同。转移的发生较低度恶性的皮质旁肿瘤多见但少于经典的中心型骨肉瘤。辅助化疗所起的作用在骨膜骨肉瘤并不明确,但是由于有约20%的发生转移的几率,多数的肿瘤治疗中心都对其应用化疗。高度恶性的表面型骨肉瘤(皮质旁骨肉瘤)传统的高度恶性的骨肉瘤也可发生于骨的表面,并且可与骨旁骨肉瘤或骨膜骨肉瘤向混淆。治疗方法与传统的骨肉瘤相同。(Fig.5)继发性骨肉瘤继发性骨肉瘤好发于患有Paget’s病和先前曾经接受放射治疗的患者。纤维结构不良而未经放疗的患者极少见继发性骨肉瘤。多中心骨肉瘤这种类型的骨肉瘤十分罕见,但是有时候患者在诊断时同时存在多个部位的肿瘤病灶,与原发肿瘤表现相似。这时候很难判断这些肉瘤是来源于多个部位或是应该被认为是转移灶。所有这样的病例,预后很差。多中心骨肉瘤也可以在治疗第一个病灶后的几年内在其它部位的骨上发生。毛细血管扩张型骨肉瘤毛细血管扩张型骨肉瘤在平片上表现为一个溶骨性的病灶伴有少量的钙化或肿瘤骨形成。在影像学上易与许多良性的病变相混淆,如动脉瘤样骨囊肿。这是一个高度恶性的,血管损害伴有少量骨样组织产生的肿瘤。患者的年龄分布和治疗原则与其它的经典的高度恶性骨肉瘤相同。虽然毛细血管扩张型骨肉瘤被认为是一种侵袭性更高的类型,但它对于辅助化疗的反应与其它类型传统骨肉瘤是相似的。通过穿刺活检获得病理诊断所需的组织常常是比较困难的,因为其通常表现为富含血管且缺乏实性区域的多囊的肿瘤组织。预后因素肿瘤侵犯的范围对于提示预后非常重要,患者有转移病灶预后较差。转移灶的存在是极差的预后因素,如果患者不能行外科治疗清除病灶,几乎没有能够长期生存的可能。对于存在的转移灶进行治疗是必须的,为的是改善患者的预后。治疗的方法包括:如有可能切除肺部的转移灶,调整化疗的方案。有时,适合于施行对于转移灶的放射治疗。原发肿瘤的部位也是重要的预后因素,因为中轴骨和四肢近端的肿瘤预后较差。肿瘤的大小被认为重要的预后因素。跳跃转移灶,指同一骨内与原发病灶相同的另一病灶,是与肺部转移相同的预后不良的指征。诊断时的病理性骨折也是不良的预后因素。对于化疗后手术切除标本的组织学坏死率的评估,是许多研究都指出的对药物反应效果的预后因素。反应差者(常被定义为坏死率小于95%)较易发生远处转移,不论是否继续进行术后的化疗,转移发生的可能高于坏死率大于95%者。原发肿瘤对于化疗的反应率作为预后因素已被多个研究的结果所证实。多种评估系统用于对经过术前化疗的手术切除的肿瘤标本进行坏死率的评估。现在,大多数认为满意的反应率为原发肿瘤的坏死率大于98%,而不满意的情况是仍然存在存活的肿瘤组织。大多数情况下,但并非全部,当患者有好的反应率时预后很好,而当术前化疗后组织学反应率不满意时往往会出现转移。化疗反应的组织学分级提供了一种在治疗过程中早期分辨患者是否有复发的高危因素的方法。其初衷是对于化疗反应差的患者增加新的药物进行挽救治疗,虽然这种愿望还未实现,但却是一个值得继续进行研究的领域。治疗化疗骨肉瘤的患者的治疗包括对于原发肿瘤进行完全的,广泛性的切除或截肢术,和全身的辅助化疗。系统性的全身辅助化疗的应用使骨肉瘤患者的预后得到了很大的改善(参见第18章关于骨肉瘤辅助化疗的专题内容)。早期的研究认为,化疗对于微小转移灶有效,所以在截肢术后应用化疗。方案包括阿霉素,大剂量甲氨喋呤,顺铂和其它一些药物,多项研究表明将无病生存率从不应用化疗的10%-20%提高到了50%-65%。化疗的好处最初并未被广为接受,尽管如此,一项比较术后即刻进行辅助化疗和延迟应用化疗(只在出现转移的患者应用)的随机研究被着手进行。其结果和其它的研究都清楚的显示进行辅助化疗的实验组有更好的无病生存率和总的生存率。最近研究的热点集中在切除肿瘤前应用术前化疗(新辅助化疗)。这种方法有几个优点,如可以根据获得的组织反应率确定预后,减小肿瘤的大小使手术更易于实施,增加肿瘤的坏死,可能有些外科医生会认为能使保肢手术更安全。由于这些原因新辅助化疗已经成为多数肿瘤中心的标准化疗方案。尽管如此,但也有一些潜在的缺点,包括可能有一些患者对于化疗反应并不好,将使耐药的肿瘤细胞增加。儿科肿瘤研究组(Pediatric Oncology Group)的一项研究表明,在总的生存率和无病生存率方面术前化疗并不比术后化疗有优势。这项研究并未得到足够的关注。儿科肿瘤研究组和儿童肿瘤研究组(Children’s Cancer Group)的另一项研究提出,在应用阿霉素,大剂量MTX和顺铂的方案中增加异环磷酰氨和/或免疫刺激剂(MTP-PE)可以有效的提高生存率,这项研究的结果尚未发表。不管化疗方案如何改进,仍有20%-40%的患者最终死于骨肉瘤。最近的研究证实了一些肿瘤对于看上去有效的治疗出现抵抗的机制。其中主要的一点原因是出现了化疗药物的耐药,使化疗药物对于肿瘤细胞不能起作用。骨肉瘤出现多药耐药的机制有多种,其中之一是P-糖蛋白。P-糖蛋白是由MDR-1(多药耐药)基因编码的一种膜结合糖蛋白,在多种肿瘤和正常组织中表达。它是一种三磷酸腺苷依赖性的膜转运糖蛋白,能够将不同分类的药物,如阿霉素泵出细胞外。有推测认为化疗反应差的主要原因是存在P-糖蛋白;当前有多项研究表明表达P-糖蛋白的肿瘤患者其无病生存率和总的生存率比在肿瘤中不能测得P-糖蛋白表达的患者要显著降低。在一项研究中,P-糖蛋白的表达与组织坏死率并不相关,并且是比肿瘤坏死率更重要的预后因素。MDR逆转剂,可以阻断P-糖蛋白功能,能使药物积聚在细胞内,以克服其副作用。不幸的是,目前的逆转剂毒性均十分显著,对于其在其它肿瘤的研究中的作用并不显著;但是克服药物耐药是目前值得重点研究的领域。确定化疗“无效者”并对其提供个体治疗避免不必要的药物毒性可能可以改善预后。手术术前化疗被认为增加了保肢手术的可能并且由于肿瘤的体积缩小可以使保肢手术更加易于实施。然而直到今天,并没有一个随机性的研究来支持这个观点,而骨肉瘤由于其基质成分,虽然可见肿瘤内的矿化,但较少见新辅助化疗后肿瘤体积的缩小。虽然如此,绝大多数的外科医生认为在化疗后切除原发的骨肉瘤从肿瘤学的观点上来说更加安全。Rizzoli研究所的一项研究证明了外科手术的边界及化疗反应(肿瘤坏死率)与局部复发危险性之间存在关系。当患者未能达到广泛性的切除和未能达到良好的化疗反应时,局部复发的危险性增加。相对的,一项儿童肿瘤研究组的近期尚未发表的长期性研究(DJ Schwartzenruber, MD, AM Goorin, MD, MC Gebhardt, MD, et al, Washington, DC, unpublished data, 1999)结果显示,对未经过术前化疗的患者施行保肢手术也可获得很好的肿瘤局部控制。绝大多数的研究中心现在都应用术前化疗对于准备进行保肢手术的患者进行治疗。不断改进的重建技术以及肿瘤外科医生不断增加的经验和自信心使得保肢手术的数量不断增加。现在,大约80%的肢体骨肉瘤患者进行了保肢手术。达到肿瘤周围正常组织的阴性边界是十分重要的手术原则,但我们并不能确切的知道所需的正常组织的厚度,许多的标本都有至少一处的邻近边缘切除的手术区域。我们需要知道的是,在下肢截肢术后的肢体功能往往很好,尤其在儿童是这样。在保肢手术中往往不能保证足够的局部控制,而局部复发又常是致命的。当能达到广泛的手术切除边界时,行截肢术和保肢术的无病生存率和总的生存率是相同的,这个结论在关于远端股骨骨肉瘤的回顾性研究中已得到证明。选择适合的患者进行保肢手术是十分重要的。所选择的手术方式不能违背肿瘤治疗的目的。虽然有些研究者报道经过化疗可以使病理性骨折愈合,以利于实施保肢手术,但病理性骨折仍可能是保肢手术的禁忌症。并没有有关对于病理性骨折后患者实施保肢手术的大量研究报告,绝大多数研究者通常选择截肢术而非保肢术,其原因是因为局部过于保守的治疗往往带来不能接受的高局部复发率。同时,出现病理性骨折患者的继发的全身转移的发生率也更高。尽管如此,那些并无移位的出现骨折的肿瘤患者,如果有好的化疗反应,也许应该是行局部切除手术的适应症。特定部位,如胫骨近段,因为难以达到足够的软组织切除边界而较难进行保肢切除手术。同样地,下肢的保肢手术对于十分年轻的还未完全发育的患者也是不适合的。这将造成他们将来出现下肢的不等长,虽然可以通过人工关节制造使之成为相对禁忌症。外科手术技术的进步使更多的患者适合行保肢手术,多种新的技术被用来修复肿瘤骨切除后残留的缺损。我们将简单谈及其中几个方面。可牺牲的骨,如尺骨、腓骨、肩胛骨和肋骨,切除后不需进行骨的重建。这些部位的骨肉瘤的手术方式已被很好的描述,而术后出现的功能障碍微乎其微。骨盆骨肉瘤的手术切除十分复杂,这里不再讨论细节。手术方式为半盆切除术或内半盆切除术。切除髂骨或耻骨支不需进行重建,而如果髋臼受累及,切除术后功能将受显著的影响。重建需采用异体骨或马鞍式关节,但其术后并发症发生率相对高而术后功能却常常不理想。许多外科医生宁愿让近端股骨和剩余的骨盆骨或骶骨间形成一个假关节,尤其是当大量的软组织被切除后。幸运的是,脊柱和骶骨的骨肉瘤十分罕见,对于其需要进行结合手术,化疗和放疗的个体化的治疗。绝大多数的骨肉瘤的保肢手术需要修复肩或膝关节结构的完整性。临床的经验集中在对于生物材料和金属关节装置的应用上。两种方法都有其优缺点,并没有有关哪一种方法更好的有说服力的对比性研究。异体骨重建可以提供重建的关节表面、韧带和肌腱附着点。假体可以提供立即的关节稳定和机械性的固定,从而允许早期的行走和使用。对于具体患者如何选择合适的手术方式取决于患者的年龄,需要修复的缺损和术者与患者本人的偏好。近端肱骨 上肢的功能只要有可能都应该予以保留。在多数病例,可以进行保留肿瘤周围正常组织的关节内或关节外切除术。这样做常常意味着丧失三角肌以及部分或全部的肩袖肌腱。肩胛盂或部分的肩胛骨可能需要切除,这完全取决于病变侵犯的范围。如果整个肩胛骨被切除(称作Tikhoff-Linberg切除术),只要保留血管神经束和正常的手的功能,其结果仍好于截肢术。关节内切除术后的重建方法包括异体骨,金属假体,或异体骨-假体复合关节。异体骨的优点在于它可以提供肩袖肌肉和其它肌肉的附着点;但是异体骨的并发症发生率较高。一项最近的16名患者的研究显示有70%的功能评分并保留了手的灵活性,但肩关节的功能也显著丧失,不能进行体育活动,脱位/半脱位,感染,骨折的发生率较高。这些作者不再使用这种方法进行重建,但仍有一些中心继续这样做。金属假体更耐用,但软组织的重建修复受到限制,肩袖的功能很差。一项有关假体重建的大样本的随访研究表明,肱骨近端与其它部位相比有最好的功能(MSTS评分系统30分中的26分)和最低的局部并发症发生率。翻修率为10%(29例中的3例)。其它研究显示常见的问题为脱位和肩关节不稳定,但肱骨的骨水泥腔松动发生率较低。异体骨-假体复合关节能够结合两者的优点而在这个部位提供最好的解决方法。对于渴望有外展功能的患者,或肩袖和三角肌被切除的患者,施行肩关节融合术应是可取的方法。异体骨移植,自体腓骨移植,或异体骨与带血管蒂的腓骨移植相结合来用于关节的融合。一项最近的研究比较了上述重建方法后患侧的手和前臂与对侧(健侧)的功能发现,对于远端肢体功能的保持水平较高,尤其是抓力和前臂旋前的力量,患者的满意程度是可以接受的。股骨的远端和胫骨的近端 对于切除膝关节周围肿瘤所积累的经验相当丰富。常常能够达到肿瘤的广泛性切除并膝关节动力的重建保留部分股四头肌的功能。关节融合术较少采用。膝关节周围的结构必须仔细的评估以确定肿瘤是否通过关节囊侵及膝关节或造成了骨折。如果有疑问,应该在手术开始时通过小的关节切口了解关节情况,并在确定关节受累后及时行关节外的切除术。在多数情况下,重建的方法包括异体关节移植,金属假体或复合关节。异体骨移植的优点在于可以保留相邻的关节的表面,在儿童可以保留骺板,但是异体骨的术后并发症发生率较高。一项近期的870例患者的长期随访报道指出,异体骨移植术后感染率为10%,骨折发生率为19%。16%的异体关节移植最终需要性全膝关节置换术,其平均的时间间隔为6年,但75%的患者其长期的功能随访(Mankin评分)是成功的。在儿童和青少年,异体骨移植能够克服金属假体的缺点,包括金属假体必须切除未侵润的骺板且有使用的寿命问题。一项104例膝关节异体骨移植的长期研究显示,5年的异体骨移植寿命为73%,而保肢成功率为93%。股骨的异体骨移植结果要好于胫骨移植,其5年的寿命分别为76%和67%。在其中86例存活2年及以上的患者中最主要的并发症为感染15%和骨折2%。化疗是影响移植骨和宿主愈合的原因,在另一项研究中指出,有49%的接受辅助化疗的骨肉瘤患者出现异体骨的不愈合。许多的并发症限制了金属假体的使用。在成人,金属假体是常用的重建方法,但是随着骨肉瘤患者的生存期的延长,必须要考虑儿童和青少年患者的假体的寿命。现在的设计应用标准的假体提高了人工关节的功能性,所以特制的人工关节已较少使用。虽然新的使假体柄更紧密贴合的设计能够增加假体的可靠性,但是最主要的潜在问题仍是假体的松动和机械性的损伤。假体表面的羟磷灰石涂层能够有效的避免松动的出现。在一项68例应用组配或特制假体重建的病例研究报告中,假体的5年生存率为83%,10年生存率为67%。12例假体进行了翻修,其中11例翻修成功。在胫骨近端的肿瘤中翻修率最高(6/13),而股骨远端的翻修率仅为10%(3/31)。11例患者(13%)出现感染,其中6例需行截肢术。胫骨近端的肿瘤患者术后的功能评分(MSTS)也是最低的。此部位假体应用的一项主要缺点是不能将膑腱有效的固定于假体上。生长发育期儿童的手术重建 由于绝大多数的骨肉瘤发生在儿童和青少年的膝关节周围,对于他们来说生长发育和肢体的功能是将来的主要问题。在应用异体骨移植治疗的患者来说,肢体的等长取决于骨骺愈合的时间或肢体的延长术。如果肿瘤位于骨干或干骺端,则骨骺有可能并未受累。这需要对于高质量的MRI进行仔细的分析,但如有可能,保留骨骺可以保留关节面和生长板 。被保留的骨骺的生长可能并不正常,但一项最近的有关儿童的研究显示,对于胫骨近段肿瘤行经骨骺的切除术后肢体的短缩小于3.5cm并常常能够达到正常的功能。这些作者采用带血管蒂的腓骨结合异体骨进行重建。另一种办法是应用可延长的假体。假体的延长方法很多,对于这种方法的经验还十分有限,但一些随访已经证实对于膝关节周围肿瘤切除术后可以达到下肢的等长。对于假体的选择取决于手术的医生。一种方法是使用标准的假体并定期调整假体体部的长度。这就需要进行多次手术并在儿童完全发育后最终更换成人假体。对于假体进行延长,由于需要切除包裹假体的纤维瘢痕组织,所以常常是困难的。现在更多的是采用新的设计使假体的延长不用通过手术就能实现。旋转成形术 这种术式适合于少儿股骨远端巨大肿瘤的患者,但有时也适用于青少年患者,肿瘤巨大,有骨内跳跃转移灶或病理性骨折,或术后希望继续进行体育活动的患者。其术后功能与膝下截肢术相同,除了其外形,易于被所选择的患者接受。让患者及其家人与一位曾经接受过旋转成形术的患者相交流或至少观看相关的录像资料并与有经验的康复师进行谈话是有意义的。在一项最近的136例患者的关于无转移的骨肉瘤的非随机性研究提示,其手术并发症的发生率较低,而术后的功能结果(MSTS)要好于其它那些保肢术。行截肢术的患者也有很低的并发症发生率,但行旋转成形术后的患者比截肢术的患者或其它各种保肢手术的术后功能更好。虽然外科医生和患者常常愿意选用其它的保肢方法,但是旋转成形术仍是十分有用一种选择。转移性骨肉瘤 对于仅存在肺转移的患者施行保肢手术可达到大约40%的生存率。各协作组不断的改进对于转移性骨肉瘤的治疗方案。并应用新的化疗药物进行II期临床实验。这些实验的目的是评价药物对肿瘤的反应率,如etoposide(VP16)和大剂量异环磷酰胺及粒细胞集落刺激因子等,都可用于转移性骨肉瘤的治疗。这些患者也可进行肺部转移灶的切除术,辅助进行化疗,所有骨和肺部的肿瘤病灶都应该手术切除。如果能达到上述条件,而且患者对于化疗敏感,则患者有30%-50%的机会可以达到长期存活,其生存率与肿瘤侵犯的范围有关。仅存在肺部转移的患者其预后要好于出现骨转移的患者。
唐顺 主任医师 北京大学人民医院 骨肿瘤科2.1万人已读 - 精选 骨肉瘤治疗 手术+化疗
☆骨肉瘤是骨肿瘤的一种吗?骨肉瘤(osteosarcoma)是一种最常见的骨原发恶性肿瘤, 好发于青少年,最常见于股骨远端、胫骨近端和肱骨近端的干骺端,病变特点是肿瘤细胞产生骨样基质,绝大部分骨肉瘤恶性程度高,易早期发生远处转移,肺转移最常见。☆什么是继发性骨肉瘤?简单的说就是继发于其他已存在的骨病变或放疗后。临床上常见的良性骨肿瘤如骨母细胞瘤,骨巨细胞瘤或动脉瘤样骨囊肿等均可继发骨肉瘤,慢性骨病,如Paget病,骨淋巴瘤放疗后也可继发骨肉瘤。☆创伤会增加骨肉瘤发生吗?目前没有循证学证据,但我们复习骨肉瘤患者病史,发现不少患者症状往往在局部受创伤后发生或者变显著的。大体原因应是骨肉瘤引起骨骼病变(如蛀虫侵蚀木头),轻微外伤即可引起疼痛甚至骨折,而对正常人来说,这些轻微外伤是不会引起典型疼痛症状的。☆骨肉瘤在青少年中最常见,是吗?骨肉瘤好发年龄有两个高峰,第一个高峰是青少年,第二个高峰是30-50岁左右成年人,我国以青少年为大部分。☆骨肉瘤导致的疼痛和生长痛有什么不同?骨肉瘤导致的疼痛往往伴有局部软组织肿块,或者早期肢体出现无痛性肿块,逐渐疼痛,其疼痛性质以夜间痛或休息痛为明显,药物一般无效或效果不佳。生长痛一般为短时间疼痛,肢体不伴有软组织肿块,同时夜间痛或休息痛不明显。简而言之,如有夜间痛,休息痛或者疼痛伴有肢体肿块就要小心骨肉瘤或者其他恶性骨肿瘤可能。☆如何自我发现骨肉瘤?骨肉瘤比较少见,难以自我发现,但青少年肢体不明原因肿胀伴疼痛,尤其是夜间痛或休息痛时,就要小心骨肉瘤或者其他恶性骨肿瘤可能,需去医院拍片或其他检查排除。☆骨肉瘤是否首选手术?手术只是骨肉瘤综合治疗中的重要组成部分之一,单纯手术并不能使骨肉瘤患者治愈,必须结合新辅助或辅助化疗才能达到良好的治愈效果,目前骨肉瘤5年治愈率一般为50%-60%。我们医院骨肿瘤科常规治疗方案为术前化疗+手术+术后化疗,必要时结合靶向及生物治疗使骨肉瘤患者达到良好的治愈效果。☆一定要截肢、去骨吗?目前随着新辅助化疗,广泛切除的保肢手术开展,我骨肿瘤科大部分初诊骨肉瘤患者可以进行保肢手术。但如果部分患者耽误时间太长或患者早期没有得到正确的诊治而使得肿瘤侵犯局部血管神经,则丧失了保肢条件。☆是否截肢,是在疾病确诊时确认,还是术前化疗后确认?截肢与否主要是根据术前全身及局部检查来判断,尤其是要结合就诊时和术前局部的MRI影像来判断,如果肿瘤侵犯局部血管神经,则丧失了保肢条件。保肢手术的适应症:Ennecking分期IIA期,对化疗反应好的IIB期,主要神经血管未受累;全身情况及局部软组织条件允许,可以达到广泛性切除;无转移灶或转移病灶可以治愈;患者有强烈的保肢愿望;经济上能够承受高额的化疗费用。总之,是施行截肢还是保肢手术,主要看肿瘤的分期与肿瘤对化疗的反应,尤其是后者更为重要。同时,辅助化疗的有效实施是保肢术的关键环节。☆保肢手术有哪些方式?保肢手术方式多样:肿瘤段切除+异体骨+人工假体;儿童可延长;关节融合术;人工假体置换;同种异体骨关节移植术;带血管自体骨移植术;肿瘤骨灭活再植术等。保肢手术的关键在于采用合理的外科边界完整切除肿瘤,广泛切除的范围包括瘤体、包膜、反应区及其周围部分正常组织,截骨平面通常应在肿瘤边缘以外125px,软组织的切除范围在反应区外1~125px。☆是否年龄越小,保肢治疗的效果越差?年龄只是一个参考,还与肿瘤侵犯范围,个体发育状况,化疗反应相关,理论讲只要适合保肢原则均可保肢,但年龄过小如5岁以下则需不同手术过渡。☆转移到肺部后,还能手术治疗吗?需根据转移部位,大小,数量及对化疗或靶向治疗的效果来综合判断,一般来讲数目不超过3-5个可手术或介入治疗。☆骨肉瘤手术前都要化疗?目前国际上的共识是术前进行新辅助化疗,但如果患者不耐受化疗、肿瘤过大或者疾病进展很快,则可根据具体病情来选择。☆长时间化疗会耽误疾病诊疗吗?一般术前行4-6次新辅助化疗就要考虑手术治疗,长时间化疗只针对无法进行手术的患者,但往往由于肿瘤没有切除,耐药等效果不佳。☆化疗是否可以增加保肢治疗的成功率?如果患者对化疗敏感,使肿瘤缩小则可增加保肢的效果与成功率。☆术前化疗会不会增加手术难度,如增加瘘的发生?术前化疗一般不会增加手术难度,但对于部分对化疗不敏感的患者,或者化疗期间肿瘤不缩小反而增大的患者,则保肢及预后效果比化疗敏感患者欠佳。☆术前化疗不敏感,要截肢吗?如果符合保肢指征,即使术前化疗不敏感也可保肢,但术后注意需改用用二线或靶向化疗药物。☆哪些骨肉瘤术后还要化疗吗?骨肉瘤术后一般建议9-12次术后化疗。☆术后化疗剂量越大越好吗?化疗药物要兼顾杀灭肿瘤与人体耐受之间的平衡,如果患者营养条件好,能耐受则可适当调高化疗药物剂量,但必须在化疗药物的应用剂量范围中应用。☆胸腺肽对于骨肉瘤治疗,有用吗?骨肉瘤化疗期间可适当应用免疫增强药物,胸腺肽不直接杀伤骨肉瘤细胞,但可增加人体免疫力,所有可作为辅助药物应用。
尹军强 主任医师 中山一院 骨肿瘤科9189人已读 - 精选 骨肉瘤、软组织肉瘤化疗---患者院外温馨提示
肉瘤化疗患者院外温馨提示化疗患者院外期间必须严密观察化疗副反应,出现严重的副反应时及时短信咨询主治教授,家属和医生的密切配合是减少防止严重副反应的最佳途径。1、观察血象:每2-3天就近到当地医院检查血常规,重点观察白细胞和血小板:化疗后7-10天(化疗用药算起)白细胞和血小板会降到最低。白细胞在2.0×109个/L以上基本安全,短效生白针剂可以使白细胞在1-3天内升高,常用药物是短效生白针剂100ug,皮下注射,40C冰箱内保存。白细胞降至2.0×109/L以下,注射短效生白针100 ug并且严密观察(隔天查血);白细胞降至1.5×109/L以下,注射短效生白针300 ug并且严密观察(隔天查血);白细胞降至1.0×109个/L以下,连续六天注射短效生白针600 ug并且严密观察(每天查血),白细胞降至0.5×109个/L以下,回院就诊。血小板降至100×109个/L以下,连续3天注射升血小板针3mg并且严密观察(每天查血); 血小板降至50×109个/L以下,连续6天注射升血小板针6mg并且严密观察(每天查血);降至30×109个/L,回院就诊。对于实在没有条件检查血常规的患者,建议经验用药:每天注射短效生白针100 ug。2、对于老年人、体质差、吃饭困难、反应重、化疗后1-5天白细胞迅速下降的患者要倍加小心。这类高危人群可以建议化疗后48小时使用长效生白针。3、院外期间注意多休息,多进食营养丰富容易消化的高蛋白食物,如牛奶、蛋鸡、鸡、鸡肝、猪肝、瘦肉和鱼。如清炖陈皮瘦肉碎,汤肉一起吃。遇到严重呕吐或口腔溃疡、不能喝汤,及时就近到当地医院输液治疗或回院就诊。4、 化疗间期休息时间从1周到3周,一般而言,术前化疗必需严格遵守化疗间隔时间,从化疗第一天算起,使用MTX(黄或橙)后间隔1周,使用ADR+DDP(红)后间隔2周,使用IFO(白)后间隔3周。具体时间咨询主管医生。5、入院前查血常规可以节省住院时间,入院手机短信预约床位。6、紧急情况或逐渐加重的副反应及时联系主管教授,必要时需要尽快回院治疗。对于高热合并严重的白细胞和血小板减少患者的经验用药:每天300 ug吉粒芬、每天丙种球蛋白5克、每天三次舒普深1克、大量补液、退热和输血,输血或血浆见效快。
王晋 主任医师 中山大学肿瘤防治中心 骨与软组织科9677人已读 - 精选 骨转移癌治疗专家共识
中华医学会骨科学分会骨肿瘤学组一、骨转移瘤概述骨骼是恶性肿瘤常见的转移部位,恶性肿瘤病人尸检结果显示骨转移瘤总体发病率为32.5%。骨转移瘤的发病率约为原发恶性骨肿瘤的35-40倍,是骨科医生经常遇到的问题。(一)临床特点骨转移瘤好发于中老年,男女比例约为3:1,多数病例为多发骨破坏。脊柱、骨盆和长骨干骺端是骨转移瘤好发部位。常见临床表现包括:①疼痛(50%-90%);②病理性骨折(5%-40%);③高钙血症(10%-20%);④脊柱不稳和脊髓神经根压迫症状(性病灶会出现自愈倾向,因此对肾癌骨转移的预防性内固定应采取积极态度。5. 甲状腺癌骨转移:甲状腺癌的骨转移仅次于前列腺癌和乳腺癌,约占60%。由于甲状腺癌恶性程度差别很大,所以甲状腺癌骨转移的临床及X线片表现较特殊。甲状腺癌骨转移病灶溶骨破坏程度往往非常严重,病理性骨折的发生率很高,预防性内固定可有效预防骨折发生,术后可配合131I内照射或放疗,预后良好。表1 常见肿瘤骨转移的发生率和预后来源骨转移发生率(%)中位生存期(月)5年生存率(%)骨髓瘤95-1002010乳腺癌65-752420前列腺癌65-754015肺癌30-40
唐顺 主任医师 北京大学人民医院 骨肿瘤科3万人已读 - 精选 侵袭性纤维瘤
概念:侵袭性纤维瘤病又称韧带样型纤维瘤病、韧带样肿瘤、肌肉腱膜纤维瘤病 。Farlances于1832年首次描述此疾病, 随后Mueller将其命名为硬纤维瘤病, Kiichols提出其可发生于身体任何部位。2006年世界卫生组织 (WHO) 新版肿瘤分类中, 将该疾病定义为软组织中间型肿瘤。 侵袭性纤维瘤病是一种起源于深部软组织的纤维母细胞克隆性增生性病变, 主要见于肌肉内结缔组织及其被覆的筋膜或腱膜, 常向邻近肌肉组织或脂肪组织内浸润性生长, 通常手术切除后容易复发, 但一些病例可出现疾病稳定和自行消退现象。 病因:侵袭性纤维瘤病病因尚不清楚, 可能是遗传、内分泌和物理等多方面因素共同作用, 导致结缔组织生长调节缺陷。伴有Gardner综合征的侵袭性纤维瘤病患者呈家族性发病, 提示本病有遗传学基础。它常发生于妊娠期或妊娠后妇女, 提示内分泌因素可能参与肿瘤生长过程, 因此临床上常采用雌激素受体阻滞剂和芳香化酶抑制剂来治疗。此外, 约25%的侵袭性纤维瘤病患者局部病灶有创伤史。近期研究显示, 侵袭性纤维瘤与胃间质瘤 (无论腹外, 还是腹内) 在肿瘤生长过程中可能有一些共同基因起作用。 发病部位:侵袭性纤维瘤可发生于全身各处, 上下肢近端和腹部为其好发部位。根据侵袭性纤维瘤病发生部位不同, 可分为腹外纤维瘤病、腹壁纤维瘤病、腹腔内和肠系膜纤维瘤病3大类。腹外纤维瘤病预后较差, 复发率可达40%~60%, 主要发生于肩部和上臂、胸壁和背部、大腿和前臂, 头颈部较少见。腹壁纤维瘤病多起自于腹壁的肌腱膜结构, 尤其是腹直肌、腹内斜肌及其被覆的腱膜。腹腔内和肠系膜纤维瘤病常起源于盆腔和肠系膜。 临床表现:典型的腹外纤维瘤病表现为深在、界限不清的质硬肿物, 常无明显诱因下发现而就诊, 微痛或无痛。有些病变可为多灶性, 少数病变可引起关节活动度受限, 侵及神经时可引起疼痛或麻木等临床症状。临床上腹外纤维瘤病很少发生恶变及远处转移。典型的腹壁纤维瘤病见于年轻的妊娠期女性或产后女性, 以产后1年以内更为多见。盆腔纤维瘤病表现为缓慢生长的肿物, 一般无明显症状, 当肿物增大时可被触及, 常被误诊为卵巢肿物。肠系膜纤维瘤病可为零星病例, 也可呈家族遗传性, 此时常伴有Gardner综合征。该类患者大部分表现为无症状的腹部肿物, 有时可出现轻微腹部疼痛, 偶见出血或肠穿孔引起的急腹症。 手术切除是侵袭性纤维瘤病的一线治疗方法, 根据手术方式不同, 可分为肿瘤内切除、肿瘤切除和根治性肿瘤切除, 相应的切缘结果分别是R2、R1和R0。目前研究报道的侵袭性纤维瘤病单纯手术有效率变化很大。Wood等 总结了近20年的相关文献, 发现侵袭性纤维瘤病手术有效率在13%~76%之间变化, 这可能由研究病例之间的差异造成。 侵袭性纤维瘤手术切除后预/侵袭性纤维瘤手术切除后预后影响因素有肿瘤部位、大小及手术切缘等。年龄大、腹外肿瘤、肿瘤体积大可能是侵袭性纤维瘤病预后不佳的独立危险因素 。 目前手术切缘对于侵袭性纤维瘤病预后的影响仍存在很大争议。Leithner等 报道了包含260例侵袭性纤维瘤病的Meta分析, 对比R1、R2和R0不同切缘侵袭性纤维瘤病术后复发情况, 认为手术切缘是肿瘤复发的重要因素。但Phillips等对109例侵袭性纤维瘤病患者进行随访观察, 发现手术切缘与复发没有明确的相关性。 2.放疗 由于侵袭性纤维瘤手术复发率较高, 放疗被用于其临床治疗, 尤其对于采用R1、R2手术切除及姑息性疗法的患者。 3.内分泌治疗 侵袭性纤维瘤病治疗模式在21世纪后开始转变, 药物治疗被广泛应用。因为侵袭性纤维瘤病在孕期妇女中较多发, 雌激素被认为与侵袭性纤维瘤病发生有关。雌激素受体调节剂他莫西芬、托瑞米芬等被应用于治疗侵袭性纤维瘤病。Bocale等报道168例采用雌激素受体调节剂 (托瑞米芬、他莫西芬) 治疗侵袭性纤维瘤病的效果, 总体有效率为51%;对他莫西芬抵抗的患者改用托瑞米芬可能有效, 这种对不同内分泌药物产生不同反应结果可能揭示了侵袭性纤维瘤病具有多样性的特点。 4.抗炎治疗 侵袭性纤维瘤病的抗炎治疗通常是单独应用非甾体类抗炎药 (西乐葆、双氯芬酸等) 或与内分泌药物联合应用。 5.干扰素治疗 6.化疗 7.靶向治疗 8.“等待观察”治疗 侵袭性纤维瘤病“等待观察”治疗是治疗模式中的新方式。Salas等 研究报道, 对27例侵袭性纤维瘤病进行“等待观察”治疗, 随访27个月, 其中6例 (22.22%) 出现进展, 5例 (18.52%) 出现肿瘤自发性消退, 提示侵袭性纤维瘤病在生长过程中存在静止期, 表明“等待观察”治疗是可行的。
马益民 主任医师 江苏省人民医院 骨肿瘤科1.6万人已读 - 精选 转移性骨癌的诊治
恶性肿瘤高居近年来国人十大死因之首位,成为医疗的重大课题。新近研发诸多新式诊断技术和治疗方式,使临床上得以早期诊断和治疗癌症,有效控制病情,改善病患功能,增长存活期间和提高生活质量,但同时会增加肿瘤转移到远处的风险。骨骼是恶性肿瘤经常发生转移的部位之一,临床上经常转移到骨骼的癌症包括前列腺癌,乳癌,肺癌,肾细胞癌,甲状腺癌,黑色素瘤等,其他如肝癌,鼻咽癌,结肠癌、膀胱癌等也会发生。骨骼转移癌症在临床上并不少见,初期病患可能因疼痛症状接受各种治疗,任何医疗专业人员都可能有机会遇到。骨骼转移癌症常会严重破坏骨骼结构而引起剧痛、病理性骨折、功能障碍,导致严重并发症;因此在治疗骨骼转移癌症病患时,须及早诊断和治疗,定期追踪病情,以免发生严重后果。本文将讨论骨骼转移癌症的特征,包括好发部位,病理生理学特征,临床症状与征候,临床评估检查,治疗方式,因康复治疗对改善骨骼肌肉系统症状上功效显著,接受康复治疗的病患日渐增多,康复治疗师也可能会在实务作业上遇到骨骼转移癌症病患的挑战,增加对骨骼转移癌症病患情况的了解,有助于早期转诊及治疗,成果才会良好。关键词:骨骼转移、临床诊治、病理性骨折骨骼转移癌症概况近年来肿瘤病患数目急速增多,根据卫生部统计资料显示,癌症高居国人十大死因之首,成为医疗的重大课题。诸多新式诊断影像技术和治疗的进展,使癌症得以早期诊断,并接受早期治疗,对于许多原先束手无策的肿瘤,已达到有效控制,改善功能,提升存活率和生活品质的成效,并延长许多肿瘤病患存活时间,但也因而增加肿瘤转移到远处的机会。在发生肿瘤转移的部位中,以肺部、肝脏和骨骼最为常见。一般认为这些转移病变系由于肿瘤细胞经由血行转移所致,但新近癌症干细胞的观念,对转移病变的致病因则有不同的见解。无论如何,临床上发生骨骼转移病变的病人数目快速增多是不争之实,且远多于骨骼的原发性恶性肿瘤。临床上经常转移到骨骼的癌症包括前列腺癌,乳癌,肺癌,肾细胞癌,甲状腺癌,黑色素瘤等,其他如肝癌,鼻咽癌,结肠癌等也会发生。病理解剖检查发现各种肿瘤发生骨骼转移发生率不同,依序为乳癌(73%),前列腺(68%),甲状腺癌(42%),肺癌(36%),肾细胞癌(35%),1其中前列腺和乳癌的高盛行率和相对存活时间较长,因此最常引发骨骼转移,2确实对当今医学境造成很大的课题。骨骼转移癌经常严重破坏骨骼,引致剧痛、骨折,造成严重功能障碍或压迫脊髓,导致严重并发症;其治疗方式众多,包括症状控制药物和双磷酸盐药物、体外放射治疗、手术(治疗病理性骨折及脊髓压迫等)、康复、抗癌药物治疗(如化学治疗、激素治疗、靶向治疗等)等,结合各专科领域的专家共同诊治,成果才会良好。3-7因此在治疗骨骼转移癌症病患时,必须及早诊断和治疗,且应定期追踪病情,以免发生严重后果。这些病患在临床上并不少见,且可能因为初期的疼痛症状接受各种治疗,任何医疗专业人员都可能会有机会遇到。目前康复治疗在改善骨骼肌肉系统的症状上功效明显,许多病患常会接受康复治疗以改善其症状,康复治疗师对于骨骼转移癌症病患的情况若可增加一些了解,应有助于早期转诊及治疗。本文将简要介绍骨骼转移性癌症及病理性骨折的相关诊治现况及新进展,包括骨骼转移癌症的症状评估,影像检查,骨盆、长骨及脊椎等处病理性骨折的风险,及相关手术的原则及应用,以供患者参考。骨骼转移癌症好发部位与病理生理学特征骨骼转移的影响因素很多,包括血流力学(血管分布、血管含量、血流量、血流速度等),癌细胞生物特性(增殖功能、对破骨细胞的调控、附着能力、穿透能力、分泌生长因子的种类及功能等),肿瘤病患存活时间等,使骨骼转移具有许多变异性。8-11骨骼转移癌经常侵犯中轴骨(脊椎、骨盆、肋骨)及四肢长骨近端,膝部或肘部以下的肢体远程也会发生,但较为少见。由于脊椎和四肢长骨为承重的骨骼,因此在病患进行日常活动时,经常会因为荷重而引起明显剧痛,甚至于发生骨折。由于骨骼转移性癌症会侵蚀骨骼,分解骨骼及基质,破坏骨骼结构,宿主骨骼也会对转移而来的外侵细胞发生不同反应,通常包括新骨合成和骨膜增生反应,以期修复被破坏的骨骼,但由于新合成的骨骼未及进行骨再塑作用,通常结构松散且生物强度较差。当病况进展快速时,转移到骨骼的癌细胞会分泌骨基质分解酵素,或分泌细胞动力素来激活破骨细胞,进而快速破坏局部骨骼,10,12若是该破坏或吸收变化的速度大于宿主的新骨形成速度时,受侵犯的局部骨骼会呈现侵蚀外观,可能为广泛的浸蚀或局部区域的破损(溶骨性病灶 osteo-lytic lesion),使骨骼结构受到破坏,骨强度即会变差,容易因轻微外伤力量而引起骨折,即病理性骨折;反之,若宿主的新骨合成速度或骨膜增生反应大于局部的骨骼破坏时,受犯部位的骨骼量会增加,呈现局部增生现象(成骨性病灶 osteoblastic lesion),可是这些增生的骨骼并未具有良好的骨骼结构分化,骨骼强度仍会降低;有些病患的骨骼转移则呈现混合性的病灶,即溶骨性病灶和成骨性病灶并存,但由于骨再塑过程为动态的生理过程,因此这些病患的骨合成和骨吸收之病理切片检查及骨代谢生化指标,皆会呈现两者活性增高的变化。10,11,13骨骼转移性癌症的临床症状与征候由于骨骼具有支撑身体、运动、保护脏器、造血及代谢的五大基本功能,前三大功能皆与骨骼完整结构与强度有明显关系,一旦发生骨骼转移性病灶,破坏骨骼完整结构后,容易发生侵蚀、破坏及骨折,引起种种症状,且行动功能也常会受到明显的抑制。肿瘤经常会影响骨代谢,有些肿瘤的治疗方式(如化学治疗或放射治疗等)会影响造血功能,经常会引起贫血、白血球数目太低等临床症状,这些都是癌症合并骨骼转移癌症导致常见症状与征候的原因。骨转移会造成相当多且严重的并发症,包括如疼痛、运动功能障碍、局部肿块、病理性骨折、背痛、高血钙、脊髓压迫和神经根压迫、以及癌细胞浸润骨髓等。常见临床症状和征候包括下列数种: 1.骨骼转移癌症患部疼痛:骨骼受到转移癌症侵蚀破坏时,会损坏局部骨骼结构,局部膨大,使骨膜受到膨胀的肿瘤挤压,造成严重疼痛,肿瘤部位剧痛是骨肿瘤的最常见症状,虽然依据剧痛期间,疼痛部位、频度、与活动关系,以及其它疼痛特征等,可供临床上臆测可能病况,但因为与许多骨骼疾病的疼痛难以分别,常令诊断发生混淆,临床上难以只根据疼痛症状来确定诊断骨肿瘤,有时并不容易区别肿瘤与一般骨骼疾病,因此偶而会延误诊断,必须提高警觉,须要求病患定期接受追踪病情进展为宜。3,14,15骨骼转移癌症的疼痛情形依受犯骨骼的情况而定,依各骨骼的功能需求及破坏程度而异,通常与骨骼发生断折(微骨折或骨折),及对局部骨膜刺激有关。举例而言,颅骨被侵犯时会引起头痛,严重时会影响意识;肋骨受到侵蚀时会引起胸部疼痛,脊椎转移会引起背痛,若再合并压迫性骨折,则可能压迫神经根或脊髓,造成局部神经根分布区域的疼痛症状。转移性骨癌的背痛很常见,通常为广大范围而不易定位痛点;痛点常位于深部,偶而会伴随不舒适感,常在夜间加剧,且平躺或休息姿势也未能缓解;有些转移性骨癌的病患因为脊椎结构不稳定,也会造成背痛,其背痛特色为平躺时较舒服,但坐立、站立及行动时,则令疼痛加剧。评估背部疼痛根源于肿瘤破坏时,可利用化疗或放射治疗控制病情,但若由于脊椎结构不稳定,则前述疗法未必可见效,此时重建脊椎的稳定度即非常重要,应由专科医师评估病况及适当选择病人及术式,以达到良好疗效。3,15若恶性肿瘤转移到上肢骨骼时,容易引起疼痛、肿胀和压痛,且会影响日常生活动作等;发生下肢骨骼的转移癌时,初期症状以疼痛为主,且疼痛会因病患行动而加剧,甚至于会影响病患的行动。这些疼痛症状的时间和发作情形也会因治疗产生一些反应变化,在临床上应多注意。一般病患若接受康复治疗一段时间,病况未见改善者,应注意再详细评估是否有其他可能因素(如转移癌),以免延误病情。 2.运动功能障碍:骨骼转移癌症病患经常会发生活动功能的障碍,这些症状可能与神经系统受压迫或肿瘤引起剧痛有关,如脊椎肿瘤破坏脊椎后,直接压迫到脊髓,影响病患的活动及感觉功能,四肢长骨受转移肿瘤侵蚀引发病理性骨折时,也会造成相关运动功能的障碍。许多病患在发生严重运动功能障碍前,可能会有一些相关的疼痛症状,尤其因为骨骼转移癌症经常会侵犯四肢长骨、脊椎骨及骨盆,这些与运动功能关系密切,在评估病患时,更应注意检查这些部位,由于临床上康复治疗常常需治疗较长的疗程,病患在接受治疗过程中,难以立即判定明确的疗效,但若在病患接受一段时间康复治疗后,结果未见改善病况时,更应再详细评估。若是在治疗疗程中,病患出现神经功能障碍的紧急症状,例如以脊椎压迫性骨折为例,当病患的背痛在治疗过程中逐渐加剧,且在腹压增加(如咳嗽、腹部出力)时更加重;有时也会伴随神经根(nerve root)疼痛,更须进一步评估是否出现无力、麻痹现象或是感觉异常现象,严重者更会发生大小便失禁,此时需施行紧急手术予以治疗。 3.局部肿块:转移性骨癌经常是多发性,在发生部位会引起疼痛,且出现局部肿胀的现象,相较于一些良性的骨肿块,由于疼痛症状不明显,可能会等肿块长得较大,才会引起注意。转移性骨癌的局部肿块大小及数目,依肿瘤种类、转移早期或晚期而异,有些恶性肿瘤的生长速度快速,很早即造成骨骼严重破坏或骨折,较少形成巨大肿瘤,但由于出血肿块,常会使患部皮肤肿胀瘀青,甚至于溃烂出血,应多加注意防范。 4.病理性骨折:转移性骨癌的肿瘤细胞常会破坏骨骼的骨小梁或骨皮质,先发生显微骨折,逐渐进而破坏骨骼结构,并减弱强度,引起病理性骨折。研究发现,乳癌病患首次复发于骨骼系统的比例约为 30%,其中 16%病患会发生长骨病理性骨折, 3%病患病患发生脊柱压迫性骨折。 16多发性骨髓癌(mutiple myeloma)也经常会发生脊椎骨折(54%)。17临床上发生病理性骨折的部位经常位于脊椎、股骨近端、肱骨近端及肋骨等,通常很小的外力即引发病理性骨折,如有些病患从X光检查台或心电图检查台下来时发生骨折,有时在穿裤子时因为单脚站立支撑身体,即会引起转移性骨癌患部骨折,有些病患在打开门窗橱柜时发生肱骨骨折,难以防范。脊椎骨折会导致患者身高变矮,脊椎侧弯,压迫局部组织或肺脏,导致功能障碍,临床上常需施行手术或相关处置才能改善病况。病理性骨折的发生风险会依骨转移时间增长而逐渐增高。临床上已发展出种种评估方式,例如根据股骨疼痛、病灶部位、病灶大小、及 X光片病灶特色,可供预估发生病理性骨折的风险,必要时需建议施行预防性内固定手术,以减少并发症的发生。18其他非特异性症状与病患的基本肿瘤有密切关系,转移性癌症病患也经常会合并出现原本肿瘤的特有症状,如肺癌引起咳嗽、肝癌出现黄疸、腹水等;其他如体重减轻、体力不支、肌肉无力、贫血、食欲不振、轻度发烧、或腰酸背痛等,有些症状与病患的化学治疗或放射治疗有关,根据这些症状并不易确定诊断;且在治疗过程中会出现一些偶发的情况而增加症状的复杂度,因此接受长期治疗而仍未改善症状时,应高度警惕,以期望减少误诊机会。有些转移性骨癌病患会出现高钙血症(hypercalce-mia),经常会引起严重并发症如心悸等,应多注意,常见引起高钙血症的肿瘤包括乳癌(17%)或多发性骨髓癌(33%),16,17其他如肺癌、肾脏肿瘤,和淋巴瘤(lym-phoma)等。有些肿瘤病患会出现副甲状旁腺素相关胜肽(PTHrP, Parathyroid hormone related peptide)上升,导致全身破骨细胞活性增强,使骨吸收量增高,导致高血钙,并非只是局部骨骼受破坏所致。12高血钙的临床症状通常并不明显,临床上需具有高度警觉性,较严重时会出现无力感、嗜睡、口渴、呕吐、恶心、便秘、脱水,更严重时会导致肠胃系统、肾脏功能甚至神经系统的障碍,如胰脏炎、意识混淆,甚至昏迷、心律不整,或因而死亡等,应小心注意。骨骼转移性癌症的临床评估临床上评估病患时,应随时提高警觉,注意发生骨骼转移性癌症的可能。有些病患在接受检查时,常常都已为肿瘤末期,肿瘤变得很大或广泛转移到各部位,严重影响预后。临床上诊查癌症病患时,应详细询问病史,施行完整身体检查,例行生化血液检查,及注意追踪本源肿瘤的变化,取得最完整数据。此外应配合完成必要的检查,这些依病况需要作适当选择,如对转移部位安排一般X光片检查,评估局部病灶的情形及发生病理性骨折的风险;胸部 X光检查,以评估肺部是否出现肿瘤、或发生肺部转移;骨骼同位素扫瞄,以供评估有无多处骨病灶;计算机断层扫瞄检查,以供评估肺、肝或肾脏肿瘤、肺部转移;磁振造影扫描检查,评估局部病灶情形、骨髓侵犯范围、骨膜反应、以及发生病理性骨折的风险;其他检查例如脊髓造影检查(评估脊髓或神经根病变);血管摄影检查(评估血管分布);神经传导速度检查或肌电图检查(判断肌肉神经病变);超音波检查(简易评估肿瘤的情形)等。3,15血液检验包括一般生化血液检查肿瘤标志检查分析等,都应依病况需求安排。最重要的诊断根据为切片检查(biopsy),此乃是肿瘤诊断的根本。骨骼活体切片检查为取出部分骨肿瘤组织,进行病理组织切片检验,可供诊断和作为治疗方针的参考;分为针刺取样和手术切开取样等两种技术,依医师经验、技术及设备等选定。临床上诊断为转移性骨癌的情形有两种,其一为已确知病患罹患肿瘤病史,当其出现多处部位症状时,通常会先视为该原发肿瘤产生转移病灶予以处理,可是临床上仍会有些例外情况,如同时并发多种不同原发性肿瘤,应加注意,诊治前的基本影像评估,生化检验及病理切片诊断仍为必须的检查。对于原发癌部位,可依需要进行检查,如肺部或内脏超音波检查、内视镜检查(上消化道,下消化道,膀胱镜等)、耳鼻喉系统检查、泌尿系统检查、妇科肿瘤检查、骨髓穿刺检查等。其二为当病患先前并没有肿瘤病史,且首次出现单一蚀骨性病灶,此时应施行完整的全身检查,包括针对常见的原发肿瘤部位进行检查,如甲状腺、乳房、前列腺,在切片外须安排其他检查项目,如骨骼病灶的 X光检查,胸部 X光检查,胸/腹部计算机断层扫描,骨骼同位素扫描检查检查,磁振造影检查等,如前述。临床上有些病患虽经诊断为转移性骨癌,但却未能在短期间内查出原发的部位,应再持续追踪,有些病患需经一段时间后才能查出原发肿瘤的部位。若只凭经验或直觉认定蚀骨性骨病灶都是转移性肿瘤,太过于自信而未先进行切片检查,即径行肿瘤刮除及内固定手术,一旦发现为原发性骨肿瘤,如骨肉瘤(osteosarcoma),则会造成局部伤口内的肿瘤细胞污染周围组织,无法进行广泛范围的切除手术,甚至于导致癌细胞扩散到远处器官,引起局部复发和转移,终致需施行截肢,甚至死亡。转移性骨癌的治疗方式针对转移性骨癌的现代化治疗,必须整合多元化全方位的治疗方式,治疗的目标在于控制病况的进展,恢复功能及改善生活质量,若是已发生病理性骨折,更须达到清除肿瘤,达到稳定固定及骨折愈合的目标,尤其因为转移性骨癌的相关范围很大,肿瘤会造成很大的侵蚀结果,且会继续破坏骨骼,因此早期诊断与及有治疗是首要原则,必要的术后治疗如化疗、放射治疗等也有助于控制病情的进展,因此治疗团队的整合是必需的。3,15治疗转移性骨癌须同时兼顾原本肿瘤的治疗与控制,而治疗转移性骨癌时,则依发生部位,局部病况,发生骨折与否,对治疗的反应等,各有不同的治疗方式。4一般而言,转移性骨癌的治疗方式可分为 1.非手术治疗:包括放射治疗、化学治疗、激素治疗、靶向治疗及其他方式等。这些治疗方式大都系针对原发部位的肿瘤,但对于发生转移性骨癌的部位,若位于不便施行的部位,病况不佳不适合手术时,或病况尚不需施行手术时,这些治疗可当做主要的治疗方式,或若需接受手术时(如发生病理性骨折时),也可作为手术后的辅助治疗。 (1)放射治疗:即使施行手术,大部分的转移性骨癌也经常未能完全根除,适当配合使用放射治疗,可更有效控制肿瘤的成长,预防发生病理性骨折,也可减轻转移部位的疼痛,施行手术后的局部放射治疗,也可用于控制局部肿瘤的成长,延长骨折固定作用。有些肿瘤如淋巴瘤,来自乳房、肺脏和甲状腺的转移性骨癌,对放射治疗的反应很好,放射性碘治疗对甲状腺转移癌瘤也具有一定疗效,但若发生转移性骨癌的位置为荷重部位,且评估后可能发生病理性骨折的机会很高时,若病人状况适合,则应建议手术后并用放射治疗为宜,以免发生病理性骨折。 (2)化学治疗、激素治疗、和/或靶向治疗:通常用于治疗原发部位的恶性肿瘤,此时并非针对转移性骨癌而言,当原发性肿瘤合并发生骨骼转移时,施行这些治疗,可同时控制部分骨骼的病况,常会一并采用。对化学治疗有反应者(如淋巴瘤),对激素治疗有反应者(如前列腺癌或乳癌等),可根据原发肿瘤的特性,适时合并使用。但应注意追踪病况。 (3)其他:例如采用双磷酸盐类药物作为辅助疗法,例如使用 pamidronate作为乳癌病患的化疗辅助疗法,可有效抑制骨骼转移、改善疼痛。5,19-21近年来亦证实采用磁振造影导引之聚焦超音波手术( MR-guided focused ultrasound surgery,MRgFUS),对于转移性骨癌的疼痛有明显的改善效果。22-24 2.手术治疗,转移性骨癌的发生部位不同,有些部位不需手术治疗,如肋骨、颅骨等,有些部位则须手术治疗,如股骨、脊椎,依病况而定;尤其是四肢骨骼且已经发生病理性骨折的患者,或是脊椎压迫性骨折且合并神经功能障碍或肢体无力的病患,此时应选择适当手术式,可使病患恢复相当程度的功能,改善生活质量。手术应以简单有效为原则,若病患经长期治疗后体弱多病,更不宜采用复杂手术,以免引起诸多并发症。治疗转移性骨癌时,应先评估病患的情况,评量肿瘤侵蚀的范围,判定手术风险及合适术式。尚未发生骨折的较大的转移性骨癌病灶,以清除肿瘤为主要治疗目标,此时骨骼结构保持完整,手术难度较小,病患术后复原较快。若发生病理性骨折,则应兼顾肿瘤切除、骨折整复与稳定固定、恢复行走功能与减轻疼痛的治疗原则,但术后约 15%会发生全身并发症,以肺炎、静脉栓塞及肺栓塞为主;也会发生局部并发症,如关节脱臼及伤口感染。7发生病理性骨折若未治疗很少能达到骨折愈合,发生病理性骨折未必表示毫无治疗希望,若适当选择手术式及固定器材,再辅以放射疗法及化学治疗,抑制肿瘤继续长大和破坏骨骼,可缓解疼痛和恢复其活动功能。手术治疗病理性骨折主要目标乃在于减少其他并发症的发生,重建稳定性和功能良好、且不疼痛的肢体,相对延长病患的存活期。若要能达成目标,需依病理性骨折的部位选用合适器材重建,常用者包括内固定器材或人工关节置换,内固定器材常用于长骨骨干或干骺部位的病灶,包括骨髓内钉,钢板与钢钉,一般需配合使用骨水泥增强固定效果。人工关节置换适应症包括:⑴内固定器材未能提供足够稳定度。⑵关节邻近的转移性骨癌,广泛侵蚀破坏关节面。⑶预期会发生骨折不愈合及相关并发症时,如股骨颈病理性骨折。若是转移性骨癌破坏范围很广,须切除大范围的骨骼及关节时,则可考虑使用订制型人工关节置换。以解剖位置而言,当下肢长骨发生病理性骨折时,若接受放射治疗无效且骨骼持续被破坏,原发性肿瘤对放射治疗及化学治疗反应不佳,使转移性骨癌病灶很可能发生骨折,即应考虑施行内固定手术,以减少手术后并发症的发生。治疗方式依部位而定,例如股骨颈病理性骨折需施行刮除肿瘤、半人工关节置换手术,若骨骼同位素扫描检查及 X光检查证实髋臼处同时受侵犯,需考虑施行全人工髋关节置换术,并以骨水泥加强固定。25,26股骨转子间病理性骨折可施行刮除肿瘤,以人工关节置换或内固定(如动力性髋骨钉DHS)合并使用骨水泥来重建。股骨转子下位病理性骨折可采用锁定式骨髓腔内钉(PFN)合并骨水泥固定。27,28近端股骨广大破坏且合并肿瘤侵犯周围软组织时,可切除整段近端股骨,并以订制型模块式人工关节重建,令病患早期恢复行走能力。但因需切除较多髋关节附近的肌肉,发生关节脱臼、关节不稳定及肌力减弱的机率较高。发生上肢长骨的病理性骨折时,须接受手术,其治疗原则相似,但因解剖构造不同,所采用的器材也有差异。其中肱骨头及肱骨颈的病理性骨折,可施行肿瘤刮除,并用半肩人工关节置换及骨水泥固定重建,破坏范围扩及肱骨近端三分之一时,可考虑使用模块式人工肩关节或复合式异体骨人工关节重建。29肱骨干病理性骨折可采用钢板或髓内钉,并在骨缺损处填塞骨水泥,加强固定效果。30脊椎发生转移病理性骨折时,若施行辅助性治疗后,脊椎发生不稳定或骨折,肿瘤持续增大并压迫神经,并发神经功能障碍,应考虑手术对脊髓及神经减压,以缓解疼痛,重建脊椎稳定性。高位颈椎病患发生转移性骨癌,且出现剧痛及脊椎不稳定时,手术主要目的为提供脊椎稳定度,不适合手术的患者,可采用牵引复位,并用外固定架(halo arthrosis)及实施放射治疗。低位颈椎发生转移性骨癌时,若肿瘤破坏一至二节颈椎,可由前位切除颈椎肿瘤,再辅以骨水泥填充骨缺损,重建颈椎稳定性,必要时可并用钢丝增强固定。受犯节数超过两节以上时,应并用后位手术增加稳定性。胸椎及腰椎发生转移性骨癌病灶时,若发生神经功能障碍时,应考虑手术减压及脊椎固定手术,以重建脊椎稳定性;可考虑施行前位减压合并前位固定来治疗,若受犯脊椎少于两节时,可施行前位减压固定,若超过两节以上,须加上后位器材固定增加稳定性。但脊椎后位手术可达成广泛减压的目标,合并良好经椎足的脊椎固定器材,可重建脊椎的稳定性,在术后配合放射治疗,效果良好,可应用在多节数广泛性脊椎受犯及后脊椎受犯情况。31康复治疗对转移性骨癌病患的意义近年来,转移性骨癌的治疗已得到广泛的重视,不但使病患的存活率增高,存活时间延长,相对于病患功能与生活质量的提高,也有很大的进展。这归功于医学诊断与治疗的进步,但肿瘤转移到骨骼系统造成病理性骨折的发生率仍一直快速增加,尤其常见于四肢长骨、脊椎及骨盆等部位。前文提及,治疗转移性骨癌的主要目标为恢复病患的功能,及早活动,减轻疼痛,发生骨折者亦应达到令骨折部位复原功能的目标。近年来手术技术的创新及辅助治疗的合并使用,使病患的疼痛和功能改善相当显著,令罹患转移性骨癌的肿瘤病患,在其疾病的末期岁月中,经由治疗可缓解疼痛,缩短长期卧床时间、改进生活质量,令病患获益良多。7,32,33康复治疗在临床诊治的角色越来越重,改善转移性骨癌病患的疼痛症状,增进功能,减少并发症的发生,这些都是很重要的贡献。相对于以往,康复治疗师的临床工作及实务相当重要,例如针对骨转移癌症的疼痛而言,对末期癌症病患除了使用吗啡,可并用经皮式神经电刺激来控制疼痛症状;34,35采用其他康复治疗方式如局部冷或浅层热疗、按摩、适量运动等,也可缓解疼痛,但不建议使用深部热疗仪器如短波或电磁波于转移性骨癌病患。针对转移性骨癌病灶可采局部按摩与关节活动,松弛僵硬的肌肉与关节,以缓解疼痛,但应注意保护发生骨骼转移病灶,必要时须使用护具如背架,辅具来保护,以减轻疼痛,增强身体功能。在转移性骨癌的处置方面,康复治疗也非常重要。可就诊断和治疗上的挑战列述如下: 1.诊断的挑战癌症病患常会因骨骼关节肌肉疼痛求诊,临床上发生转移性骨癌的病患,在临床医师施行治疗后,若因情况需要,经评估需以康复治疗方式协助改善症状时,临床医师会咨请康复治疗师来协助,医师或康复治疗师会根据病史,评估疼痛与转移性癌症的相关性,施予安全适当治疗。 35此时在诊断上已有一些根据,但在治疗过程中,宜配合临床病况追踪其变化,若经一段时间康复治疗后,症状未如预期改善时,应提醒医师重新评估病情,尤其是对于具有常发生骨骼转移癌症病史的患者,以诊断是否有新的病灶。有时对于尚未发生病理性骨折的病灶,在治疗过程中若突然发生剧痛,应注意是否可能发生病理性骨折,需及早评估治疗。可是在临床实务上,疼痛是癌症和其他病症的常见症状之一,有些接受康复治疗的病患未必在发生前会有明确的病史或资料可供评估判定。这些病患可能因为疼痛症状由医师转介求诊,且先前未必有癌症病史,例如有些病患因发生肩痛、颈痛或背痛求诊,接受数月之久的康复治疗后,由于症状未改善,甚至于发生病理性骨折后,才被诊断为转移性骨癌,且可能与症状的部位相符合,这些延误诊疗的情形往往会造成医病关系的紧张,更增高康复治疗师的临床实务难度,有鉴于此,随时保持警觉,注意治疗过程中的病情变化与症状改善情形,若康复治疗效果与预期不同,应再审慎评估,多注意疼痛型态的变化,都有利于早期转介进行检查,并及早治疗。 2.治疗:对于已知发生转移性骨癌病患的康复治疗方式及项目之选用,应依康复治疗原则而定,治疗上可分两类讨论:⑴尚未发生病理性骨折的转移性骨癌病灶康复治疗的目标在于协助病患改善症状及功能,使病患的生活质量进步,虽然转移性骨癌的肿瘤基本病况并非康复治疗所可改善,但若病灶较小,尚未发生病理性骨折时,适当的康复治疗可减轻疼痛、维护体能、协助控制症状, 33但在施行康复治疗过程中,应注意转移性骨癌病患的基本病况进展,保护病灶,避免造成医源性伤害,此外可加强训练病患的平衡功能、肌力及反应能力,指导防范跌倒及保护措施、家居环境的改善,以减少骨折风险。⑵发生病理性骨折的治疗发生病理性骨折后,局部骨骼破坏较大,手术后并发症与内固定松脱风险比一般骨折高,且常会安排术后的局部放射治疗,因此其基本治疗原则比一般骨折的原则复杂, 7即使有些部位如颅骨或肋骨的转性骨癌病灶,不需手术治疗,但仍会安排放射治疗来控制局部肿瘤生长,因此在施行康复治疗时,应注意放射治疗对于皮肤和肌肉软组织的影响。考虑转移性骨癌侵蚀破坏骨骼的部位、侵润骨质后残存骨骼的质量,病灶周围软组织受侵犯的程度,使用固定器材如钢板后肌肉附着部位经手术分离后不易贴附在钢板上,局部放射治疗影响该处的肌肉再生,以及病患经长期化疗后的体力减弱等,都会影响病理性骨折病患在手术后的复原,病患发生下肢长骨病理性骨折后,治疗目标为提供足可负荷体重的固定力,且可及早下床步行;病患发生上肢病理性骨折时,则期望治疗后可复原日常生活搬动或拉动物体的动作。因此针对病理性骨折病患接受骨折整复及内固定器材重建的病患,在实施康复治疗前,须审慎评估考虑病灶部位的稳定度,即使经手术切除肿瘤,并用骨水泥和内固定器材可强化固定力量,但因肿瘤病理性骨折的愈合差,因此需仔细评估固定力,注意保护防范,肌力训练,关节活动度的训练,辅具的适当使用,并评估病灶是否出现更扩大的侵蚀等,在考虑可否允许上肢使用助行器或拐杖来协助康复前,须评估病患的上肢功能,及可能的上肢骨转移病灶,尤其对于多发性骨骼转移病患更须如此。若病患取用皮肤移植取皮区或皮瓣来重建,设计支架时应注意对于取用部位的伤口特别保护;对于肢体需设计特殊支架,提供术后早期的支撑及活动。这些都会影响到疗效与安全,应多注意。针对使用一般式人工关节重建并用髓腔骨水泥固定的病患,可达到立即固定人工关节的效果,但施行康复治疗前仍应评估肿瘤病灶周围软组织的侵蚀对局部的影响,且需审慎追踪评估;若因转移性骨癌侵蚀范围太大,需使用模块式人工关节重建( modular endoprosthesis)并用髓腔骨水泥固定,通常会切除病灶周围的肌肉,或将肌肉重新缝合到模块式人工关节上, 27,28此时需要一段时间使软组织和肌肉生长良好,以包覆人工关节,才可提供良好活动力,因此适当保护,肌力训练,关节活动度训练,辅具使用与防范跌倒的指导都很重要,减少在术后早期发生脱臼,及日后发生人工关节松脱,以改善其生活质量和功能,这些都显现出多元全方位团队治疗,对转移性骨癌病患的重要。髋臼病患需更复杂的重建,风险及并发症更大。脊椎病理性骨折通常需穿用强化型背架,指导肌力训练,对于已发生肢体肌肉无力的病患,在脊椎手术后,需更加强肌力训练及防范褥疮。结 论近年来癌症治疗有许多新进展,令病患存活时间延长,相对使骨骼系统受肿瘤侵犯的发生率增高,引发转移性骨癌,造成局部骨骼破坏或病理性骨折,导致疼痛和功能障碍,针对转移性骨癌的诊断与治疗,也已有明显进步。临床上由于转移性骨癌病患的病况不同,康复治疗计划须针对个人订定,兼顾安全及保护骨骼,维护活动力,减轻疼痛和强化体能的基本目标,以期维持病患的生活质量,目前少有完整的实证研究资料,可据以订定适用所有转移性骨癌病患康复治疗规画,康复治疗师对癌症病患及其病程都必须熟悉才能胜任。尤其对于接受病理性骨折手术的病患,更应详细了解手术情形,依康复治疗常规与经验安排治疗。对术前和术后的病患,康复治疗运动的目标在于增强肌力和肌耐力,应告知病患避免从事高撞击和扭转的危险动作,保护骨骼避免骨折。转移性骨癌的治疗应采取团队治疗,定期检查追踪曾罹患其他癌症的病患,可及早诊断与治疗,以控制肿瘤扩展,减轻疼痛和预防发生病理性骨折,改善疗效和生活质量。第一线医护人员都应对转移性骨癌有相当的认知,尤其是面对十大死因以癌症居首位的现今,即使单纯因为疼痛接受康复治疗的病患,亦可能会面对到曾发生过癌症的病患,或可能潜在发生转移性骨癌的风险,在平日的临床实务中,应多警觉注意,以及早诊断及转介治疗。参考文献 1. Galasko C. The Anatomy and Pathways of Skeletal Metastases. In: Weiss L, GilbertA, editors. Bone metastases. Boston: GK Hall; 1981: 49-63. 2. Rubens R. Bone Metastases. In: Rubens RD, Mundy GR, editors. Clinical Oncology. 2nd ed. New York: Churchill; 2000:836-71. 3. Clark JC, Dass CR, Choong PF. Current and future treatments of bone metastases. Expert Opin Emerg Drugs 2008;13:609-27. 4. Uchida A, Wakabayashi H, Okuyama N, Okamura A, Matsumine A, Kusuzaki K. Metastatic bone disease: pathogenesis and new strate-gies for treatment. J Orthop Sci 2004;9:415-20. 5. Ural AU, Avcu F, Baran Y. Bisphosphonate treatment and radio-therapy in metastatic breast cancer. Med Oncol 2008;25:350-5. 6. Gianfelice D, Gupta C, Kucharczyk W, Bret P, Havill D, Clemons M. Palliative treatment of painful bone metastases with MR imag-ing-guided focused ultrasound. Radiology 2008;249:355-63. 7. Katzer A, Meenan NM, Grabbe F, Rueger JM: Surgery of skeletal metastasis. Arch Orthop Trauma Surg 2002;122:251-8. 8. Tobinick E, Vega CP. The cerebrospinal venous system: anatomy, physiology, and clinical implications. Med Gen Med 2006;8:53. 9. Gonzalez-Angulo AM, Morales-Vasquez F, Hortobagyi GN. Over-view of resistance to systemic therapy in patients with breast can-cer. Adv Exp Med Biol 2007;608:1-22. 10. Coleman RE. Conclusion: Bone markers in metastatic bone dis-ease. Cancer Treat Rev. 2006;32(Suppl 1):27-8. 11. Virk MS, Lieberman JR. Tumor metastasis to bone. Arthritis Res Ther 2007;9(Suppl 1):S5. 12. Morton AR. Hypercalcaemia. Albeloff MD, editor. Clinical Oncol-ogy. 2nd ed. New York: Churchill Livingstone; 2000:719-35. 13. Garnero P. Markers of bone turnover in prostate cancer. Cancer Treat Rev 2001;27:187-92; discussion 93-6. 14. Dy SM, Asch SM, Naeim A, Sanati H, Walling A, Lorenz KA. Ev-idence-based standards for cancer pain management. J Clin Oncol 2008;26:3879-85. 15. Harrington K. Spine Stabilisation. In: GR Mundy, editor. Cancer and the Skeleton. London: Martin Dunitz; 2000:245-62. 16. Coleman RE, Rubens RD. The clinical course of bone metastases from breast cancer. Br J Cancer 1987;55:61-6. 17. Kanis JA, McCloskey EV. Bisphosphonates in multiple myeloma. Cancer 2000;88:3022-32. 18. Mirels H. Metastatic disease in long bones. A proposed scoring system for diagnosing impending pathologic fractures. Clin Orthop 1989:249:256-64. 19. Coleman RE, Purohit OP, Black C, Vinholes JJ, Schlosser K, Huss H, et al. Double-blind, randomised, placebo-controlled, dose-finding study of oral ibandronate in patients with metastatic bone disease. Ann Oncol 1999;10:311-6. 20. Hultborn R, Gundersen S, Ryden S, Holmberg E, Carstensen J, Wallgren UB, et al. Efficacy of pamidronate in breast cancer with bone metastases: a randomized double-blind placebo controlled multicenter study. Acta Oncol 1996;35(Suppl 5):73-4. 21. Kohno N. Treatment of breast cancer with bone metastasis: bisphosphonate treatment -current and future. Int J Clin Oncol 2008;13:18-23. 22. Gianfelice D, Gupta C, Kucharczyk W, Bret P, Havill D, Clemons M. Palliative treatment of painful bone metastases with MR imag-ing-guided focused ultrasound. Radiology 2008;249:355-63. 23. Liberman B, Gianfelice D, Inbar Y, Beck A, Rabin T, Shabshin N, et al. Pain palliation in patients with bone metastases using MR-guided focused ultrasound surgery: a multicenter study. Ann Surg Oncol 2009;16:140-6. 24. Catane R, Beck A, Inbar Y, Rabin T, Shabshin N, Hengst S, et al. MR-guided focused ultrasound surgery (MRgFUS) for the pallia-tion of pain in patients with bone metastases-preliminary clinical experience. Ann Oncol 2007;18:163-7. 25. Van der Linden YM, Dijkstra PD, Kroon HM, Lok JJ, Noordijk EM, Leer JW, et al. Comparative analysis of risk factors for patho-logical fracture with femoral metastases. J Bone Joint Surg Br 2004;86:566-73. 26. Lane JM, Sculco TP, Zoland S . Treatment of pathological fractures of the hip by endoprosthetic replacement. J Bone Joint Surg Am 1980;62:954-9. 27. Wheeler DL, Crov TJ, Woll TS, Scott MD, Senft DC, Duwelius PJ. Comparison of reconstruction nails for high subtrochanteric femur fracture fixation. Clin Orthop 1997;338:231-9. 28. Bickels J, Meller I, Henshaw RM, Malawer MM. Reconstruction of hip stability after proximal and total femur resections. Clin Or-thop 2000;375:218-30. 29. Witting JC, Bickels J, Wodajo F, Kellar-Graney KL, Malawer MM. Constrained total scapula reconstruction after resection of a high-grade sarcoma. Clin Orthop 2002; 397:143-55. 30. Dijkstra S, Stapert J, Boxma H, Wiggers T. Treatment of patho-logical fractures of the humeral shaft due to bone matastases: A comparison of intramedullary locking nail and plate osteosynthesis with adjunctive bone cement. Eur J Surg.Oncol 1996; 22: 621-6. 31. Wang JC, Boland P, Mitra N, Yamada Y, Lis E, Stubblefield M, et al. Single-stage posterolateral transpedicular approach for resection of epidural metastatic spine tumors involving the vertebral body with circumferential reconstruction: Results in 140 patients. J Neu-rosurg Spine 2004;1:287-98. 32. Dutka J, Sosin P. Time of survival and quality of life of the patients operatively treated due to pathological fractures due to bone metas-tases. Orthop Traumatol Rehabil 2003;5:276-83. 33. Nathan SS, Healey JH, Mellano D, Hoang B, Lewis I, Morris CD, et al, Survival in patients operated on for pathological frac-ture: Implications for end-of-life orthopedic care. J Clin Oncol 2005;23:6072-82. 34.Ahmed HE, Craig WF, White PF, Huber P. Percutaneous electri-cal nerve stimulation (PENS): a complementary therapy for the management of pain secondary to bony metastasis. Clin J Pain 1998;14:320-3. 35. Twycross RG. Management of pain in skeletal metastases. Clin Orthop 1995; 312:187-96.
马益民 主任医师 江苏省人民医院 骨肿瘤科2.4万人已读 - 案例 腹盆肿瘤
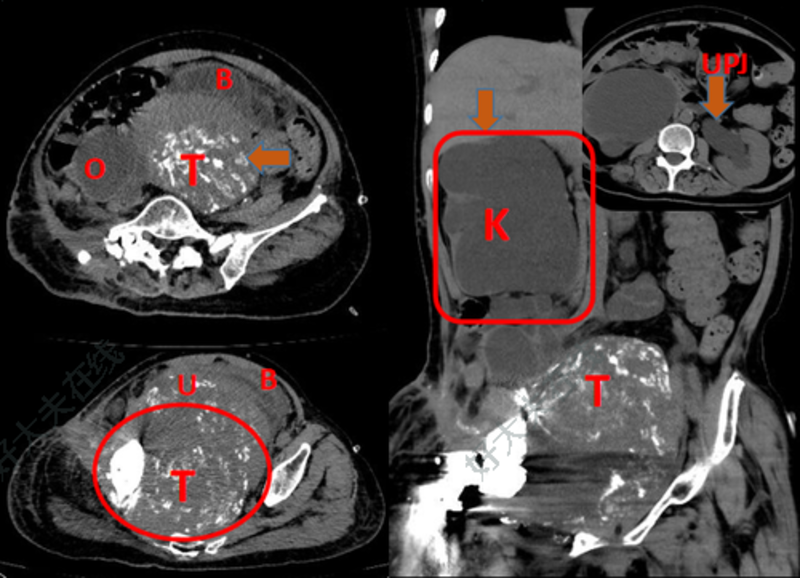
治疗前 马益民主任医师为冯阿姨进行了详细检查,查体时发现冯阿姨右臀部手术创口愈合欠佳,右下肢髋关节活动受限,下肢阵发性针刺样疼痛。经过影像病理等检查判断,冯阿姨原发的右髂部肿块其实是一种躯干型侵袭性纤维瘤,目前已经迅速进展,体积巨大,占据了整个右侧骨盆及整个盆腔,同时侵犯子宫、膀胱、输尿管,粘连肠管。右侧肾脏因输尿管长期被包裹且受压闭塞导致肾积水,已经失去功能,右下肢因肿瘤侵犯卡压骨盆部血管及腰骶部神经导致患肢长期肿胀剧痛,无法活动,左下肢出现放射性疼痛,且频率越来越高。同时由于肾功能不全导致恶性高血压、严重贫血、低蛋白血症、电解质紊乱等,严重危及生命。 治疗中 多学科联合会诊指明治疗方向 这是一例极为复杂的腹膜后累及盆底肿瘤,妥善处理需要多学科共同参与。马益民主任医师立刻汇报科主任殷国勇教授,在医务处指导下联合普通外科、肿瘤科、肾内科、泌尿外科、妇科、输血科等进行多学科联合会诊,并给出指导意见,因肿瘤累计髂骨、骶骨、腹腔多脏器,且对化疗不敏感,术前进行肾脏造瘘缓解肾性高血压,术中需行半骨盆截肢同时联合腹膜后盆底肿瘤切除、右肾及输尿管切除、全子宫切除、全膀胱切除、左输尿管造瘘、结肠造瘘等可能,必须由多学科联合进行手术,手术有生命危险,风险极大。与患者及家属沟通后,患者及家属手术意愿强烈,决定进行手术。 治疗后 治疗后7天 为冯阿姨进行多学科联合会诊 马益民主任医师表示,侵袭性纤维瘤是一种较为罕见的间叶性交界性肿瘤,分为腹外型(7冯阿姨这种肿瘤特点是良性肿瘤恶性生长,如果不切除,继续姑息治疗的话会无限制生长,继续破坏周围器官,进而危及生命。 近日,冯阿姨接受了多学科联合手术,首先由骨科马益民主任医师团队进行探查,发现盆腔内巨大实质性肿瘤约25*25*20cm大小!之后普外科血管病区马昊主任医师接力上台,仔细分离并切断缝扎右侧髂总动脉,阻断肿瘤及右下肢血供。随后骨科马益民主任医师接棒,将肿瘤自骶骨前方间隙剥离摘除,并离断右侧骶髂关节及耻坐骨,完全切除右侧半骨盆及下肢,保留臀部大部肌肉及皮瓣,之后普外科结直肠病区王勇副主任医师、妇科罗成燕主任医师、泌尿外科李普副主任医师、骨科高峰副主任医师轮流上台进行对应手术处理,术中发现结直肠肿瘤并未累及,最终保留患者的排便功能。在麻醉与围术期医学科周钦海主任医师保驾下整台手术一气呵成,共耗时8小时,术后冯阿姨病情稳定,在医护人员精心治疗下,目前恢复良好,即将出院。
 马益民 主任医师 江苏省人民医院 骨肿瘤科61人已读
马益民 主任医师 江苏省人民医院 骨肿瘤科61人已读 - 医学科普 吃“发物”会促进肿瘤生长?不可不知的肿瘤患者饮食6大误区
转自百度科学辟谣
 马益民 主任医师 江苏省人民医院 骨肿瘤科1330人已读
马益民 主任医师 江苏省人民医院 骨肿瘤科1330人已读 - 医学科普 5年生存率及肿瘤相关概念
随着癌症发病率和致死率越来越高,“谈癌色变”已成为当今社会的一个常态。正所谓:知己知彼,百战不殆,要想抗癌,得先对肿瘤的相关事项进行一定了解。然而,对于肿瘤科的很多专业词汇,很多人一知半解。 5年生存率人们对癌症非常敏感,一听到肿瘤科医生说到5年生存率,就心慌慌,吓得不行,以为自己就只有5年的时间活了。一些人在听说谁谁得了恶性肿瘤,第一句话也是“还有几年的时间”。 其实,我们很多人都对肿瘤科所说的“5年生存率”“10年生存率”产生了误解。在肿瘤科专业术语中,“5年生存率”只是肿瘤科医生用来评价癌症治疗效果的一种说法,即肿瘤病人在接受治疗后,活超过5年以上的比例。 比如说对100位接受同样治疗的恶性肿瘤患者进行术后长达5年时间的追踪,如果5年后还有20人还活着,有80人因为肿瘤复发或者肿瘤转移而死亡,这就说明这批肿瘤患者的5年生存率为20%。 无论是5年生存率还是10年生存率,这只是肿瘤科医生给出的一个参考,肿瘤患者大可不必惶惶而终日,自己吓自己。只要积极接受治疗,提高癌症生存率不是问题。 穿刺活检,软组织肿瘤诊断利器肿瘤穿刺活检是判断肿瘤为良性还是恶性的最好办法,肿瘤穿刺活检是在CT、超声的导引下,确定体内病变的具体位置的一种手段。在准确定位病变位置之后,通过局部麻醉,用细小的钢针刺透皮肤表层,命中肿瘤病灶,以此获得相关的病理组织。收集到了相关的病理组织,就可以进一步观察其形态,得出有针对性的治疗方法。 肿瘤穿刺活检的优点是方便快捷,不用开刀,也不影响早期治疗,出血少、感染几率低、准确率高达98%以上。 但是在一些对肿瘤穿刺活检不了解的人眼中,这是一件极为恐怖的事,而且随着“肿瘤穿刺活检导致癌细胞扩散”这一谣言的传播,更多人惶恐了。 要科学看待肿瘤穿刺活检,首先,人体中本来就存在上千万的原始肿瘤细胞,只是每天被免疫系统清除,所以不会形成威胁人体健康的肿瘤。而通过肿瘤穿刺活检导致肿瘤转移的更是少之又少! 肿瘤细胞分化程度恶性肿瘤高分化、中分化、低分化是按照肿瘤分化的程度来进行分级的病历等级,表示肿瘤的恶性程度。 高分化是指肿瘤低度恶性,中分化是指肿瘤中度恶性,低分化是指肿瘤高度恶性。也就是说,分化得越好,就代表肿瘤细胞越接近相应的正常发源组织。低分化或者未分化,就代表肿瘤细胞和相应的正常发源组织区别大。 高分化和中分化说明肿瘤转移少、发展慢、预后良好,低分化和无分化则相反。 肿瘤异质性是影响所有临床肿瘤内科治疗效果的一个重要因素,是恶性肿瘤的特征之一,意思是肿瘤在生长过程中,经过数次分裂增殖,使肿瘤子细胞的分子生物学或基因发生改变,导致肿瘤出现生长速度、侵袭能力、对药物的敏感性和预后等各方面的差异。 肿瘤标志物肿瘤标志物是细胞在血液中释放的一种异常物质,与肿瘤的发生、发展以及预后密切相关。癌胚抗原、甲胎蛋白等是常见的肿瘤标志物,不同的标志物关系着不同疾病的诊断筛查。 这意味着肿瘤标志物对帮助肿瘤患者早发现、早治疗、早康复有重要的意义,一是早期发现肿瘤,二是诊断与分期肿瘤,三是普查与筛查肿瘤,四是手术、化疗和放疗,五是肿瘤复发指标,六是肿瘤预后判断。 当我们读懂肿瘤科的这些专业术语之后,对肿瘤的了解便又多了一分。俗话说:“知己知彼,百战不殆。”面对肿瘤,我们需要的就是这种精神,不害怕,不躲避,往前冲,战胜它! 本文转自08-16 15:57广州启生信息技术有限公司本文为转载文章,如有侵权请联系作者删除。
马益民 主任医师 江苏省人民医院 骨肿瘤科1889人已读





